在研究性学习小组进行SO2的制备及性质探究实验中,实验装置通常包括气体发生装置、性质检验装置和尾气处理装置。以下是实验的关键步骤、现象分析及注意事项。
一、实验装置与原理
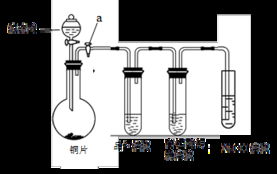
实验采用亚硫酸钠与浓硫酸反应制备SO2气体,反应原理为:Na2SO3 + H2SO4(浓) → Na2SO4 + SO2↑ + H2O。装置中,A为活塞,用于控制反应进行;加热及固定装置已略去,说明该反应在常温下即可快速发生。气体依次通过性质检验装置,最终用NaOH溶液吸收尾气,防止SO2污染空气。
二、实验步骤与操作
- 连接仪器并检查气密性:按顺序连接气体发生装置(含分液漏斗和圆底烧瓶)、性质检验装置(如品红溶液、酸性KMnO4溶液、滴有酚酞的NaOH溶液等)和尾气吸收装置。关闭活塞A,向分液漏斗中加水,观察液面是否稳定,以检查装置气密性。
- 添加药品:在圆底烧瓶中加入适量亚硫酸钠固体,在分液漏斗中加入浓硫酸。性质检验装置中分别装入对应试剂。
- 实验操作:打开活塞A,使浓硫酸缓慢滴入亚硫酸钠中,反应立即发生,产生SO2气体。通过观察各性质检验装置的变化,探究SO2的性质。
三、性质探究现象分析
- 漂白性:SO2通入品红溶液中,溶液红色褪去,加热后红色恢复,证明SO2具有可逆的漂白性,与有机色素结合生成无色物质。
- 还原性:SO2通入酸性KMnO4溶液中,紫色褪去,表明SO2被氧化为SO4^2-,体现其还原性。
- 酸性氧化物的性质:SO2通入滴有酚酞的NaOH溶液中,红色褪去,说明SO2与碱反应生成亚硫酸盐和水,体现酸性氧化物性质。
- 毒性及尾气处理:实验SO2被NaOH溶液吸收,发生反应:SO2 + 2NaOH → Na2SO3 + H2O,防止气体逸出。
四、注意事项
- 浓硫酸滴加需缓慢,避免反应过于剧烈。
- 实验应在通风橱或通风良好处进行,避免吸入SO2。
- 性质检验装置顺序可调整,但尾气吸收装置必须位于末端。
- 实验结束后,先关闭活塞A停止反应,再拆卸装置。
通过本实验,学生不仅掌握了SO2的制备和性质验证方法,还深化了对酸性氧化物、还原性及环境污染处理的理解,体现了研究性学习在化学教学中的实践价值。